| Natureduca - Portal educativo de ciencia y cultura |

Química
VELOCIDAD Y EQUILIBRIO EN QUÍMICA
El equilibrio químico - 1ª parte
El concepto de equilibrio químico
 a idea de reacción química lleva a veces a
suponer que el proceso progresa de los reactivos hacia los productos, y que se
detiene cuando se agota el reactivo que se encuentra en menor proporción. Este
tipo de reacciones se denominan irreversibles.
a idea de reacción química lleva a veces a
suponer que el proceso progresa de los reactivos hacia los productos, y que se
detiene cuando se agota el reactivo que se encuentra en menor proporción. Este
tipo de reacciones se denominan irreversibles.
Sin embargo, con mayor frecuencia sucede que, a medida que los productos van haciendo su aparición en la reacción, tanto mayor es su capacidad para reaccionar entre sí regenerando de nuevo los reactivos. Cuando esto es posible en una reacción química, se dice que es reversible y se representa mediante una doble flecha, indicando así que la reacción puede llevarse a efecto tanto en un sentido como en el inverso:
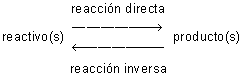
El equilibrio químico tiene un carácter dinámico, pues no implica que la reacción se paralice en ambos sentidos como podría pensarse, sino que, en cada unidad de tiempo, se forman y desaparecen el mismo número de moléculas de cualquiera de las sustancias que intervienen en el proceso. Si algunos de los productos pueden desprenderse y abandonar el sistema, se rompe el equilibrio y la reacción se verifica sólo en un sentido, hasta que los reactivos se hayan transformado totalmente.
Por ejemplo, la reacción de oxidación del hierro por vapor de agua a alta temperatura, es reversible cuando se lleva a cabo en un recipiente cerrado:3Fe + 4H2O < > Fe3O4 + 4H2
Pero debido a que el hidrógeno es un gas más ligero que el aire, si se abre el recipiente, lo abandonará, con lo cual ya no será posible el proceso inverso y el equilibrio quedará definitivamente roto.La reacción de formación o síntesis de yoduro de hidrógeno (HI) a partir de sus elementos:
H2 + I2 < > 2HI
constituye otro ejemplo de reacción reversible. Para estudiarla en el laboratorio se emplean recipientes cerrados de modo que la cantidad total de materia no varíe. Cuidadosas medidas experimentales han permitido calcular las velocidades de las reacciones directa e inversa y su variación con el tiempo. La figura adjunta representa los resultados obtenidos. La velocidad del proceso directo:H2
+ I2
![]() 2HI es importante al principio (pendiente pronunciada), mientras que la del
proceso inverso: 2Hl
2HI es importante al principio (pendiente pronunciada), mientras que la del
proceso inverso: 2Hl
![]() H2
+ I2
es casi nula. Conforme el tiempo avanza, la primera va disminuyendo y la segunda
aumentando. A partir de un cierto instante ambas coinciden, lo que indica que
entonces se ha alcanzado el equilibrio químico.
H2
+ I2
es casi nula. Conforme el tiempo avanza, la primera va disminuyendo y la segunda
aumentando. A partir de un cierto instante ambas coinciden, lo que indica que
entonces se ha alcanzado el equilibrio químico.



