| Natureduca - Portal educativo de ciencia y cultura |

Química
MATERIA Y REACCIÓN QUÍMICA
Ecuaciones químicas - 1ª parte
El balance de materia en las reacciones químicas
 artiendo de la ley de conservación de la masa y de su
relación con la teoría atómica de la materia, permiten enfocar el estudio de las
reacciones químicas como si se tratara de un balance entre átomos de una misma
especie.
artiendo de la ley de conservación de la masa y de su
relación con la teoría atómica de la materia, permiten enfocar el estudio de las
reacciones químicas como si se tratara de un balance entre átomos de una misma
especie.
Para que dicho balance cuadre, se han de introducir, con frecuencia, algunos coeficientes numéricos que permiten igualar el número de átomos de cada elemento a uno y otro lado de la flecha. Cuando esto se consigue se dice que la reacción química está ajustada, lo que significa que puede ser considerada, en sentido estricto, como una igualdad o ecuación química.
El conocimiento de las
ecuaciones químicas y la estequiometría permite la elaboración de
diferentes productos en las cantidades deseadas con las proporciones
adecuadas, esto es de suma importancia a la hora de elaborar los
medicamentos.
Dado que las masas de los diferentes átomos son conocidas, las ecuaciones ajustadas se convierten, en primer término, en relaciones entre las masas de sustancias que intervienen en la reacción. Ello hace posible la realización de cálculos químicos precisos sobre la base que proporcionan las ecuaciones químicas ajustadas, sus símbolos y sus coeficientes numéricos. Así, la reacción de descomposición del óxido de cobre (II) una vez ajustada es:

e indica que por cada dos moléculas de óxido de cobre (II) se forman dos átomos de cobre y una molécula de oxígeno. Tratando dicha ecuación química como si de una ecuación matemática se tratara, es posible multiplicar ambos miembros por un mismo número N sin que se altere la igualdad, es decir:
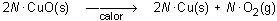
Si N representa el número de Avogadro NA o número de partículas que componen un mol, entonces la ecuación anterior puede interpretarse en términos de moles; dos moles de CuO se descomponen en dos moles de Cu y un mol de O2. Por tanto los coeficientes de una ecuación química ajustada representan también la proporción en número de moles, de reactivos y productos que participan en la reacción.
Cuando las sustancias son gaseosas, de acuerdo con la hipótesis de Avogadro, cada mol equivale a un volumen de sustancia de 22,4 litros medidos en condiciones normales de presión y temperatura. Ello significa que, junto con cálculos de masas, es posible efectuar cálculos de volúmenes en aquellos casos en que intervengan sustancias gaseosas.



