| Natureduca - Portal educativo de ciencia y cultura |

Física
CALOR Y ENERGÍA TÉRMICA
Calor y trabajo - 2ª parte
Las máquinas térmicas
 unto a la conversión de trabajo en calor puesta de manifiesto
en las experiencias de Joule, la transformación efectuada en sentido inverso es
físicamente realizable.
unto a la conversión de trabajo en calor puesta de manifiesto
en las experiencias de Joule, la transformación efectuada en sentido inverso es
físicamente realizable.
En todas las máquinas térmicas el sistema absorbe calor de un foco caliente; parte de él lo transforma en trabajo y el resto lo cede al medio exterior que se encuentra a menor temperatura. Este hecho constituye una regla general de toda máquina térmica y da lugar a la definición de un parámetro característico de cada máquina que se denomina rendimiento y se define como el cociente entre el trabajo efectuado y el calor empleado para conseguirlo. Expresado en tantos por ciento toma la forma:

Por tal motivo las transformaciones energéticas que terminan en calor suponen una degradación de la energía, toda vez que la total reconversión del calor en trabajo útil no está permitida por las leyes naturales.
Aplicación de la relación calor/trabajo
En una experiencia como la de Joule se ha utilizado un peso de 10 kg que se ha elevado a una altura de 2 m. Si el calorímetro completo incluyendo las aspas equivale a una masa de agua de 1,5 kg y la temperatura inicial es de 15C, determínese la temperatura final que alcanzará el agua, admitiendo que todo el trabajo mecánico se convierte en calor dentro del calorímetro. (Considérese el calor específico del agua c = 4,18 · 103 J/kg · K).De acuerdo con el principio de conservación de la energía, el trabajo mecánico se convierte íntegramente en calor:
W = Q
Siendo en este caso W = m g h y Q = m' c(Tf - Ti).Igualando ambas expresiones y despejando Tf se tiene:
m g h = m' c(Tf - Ti)
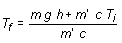
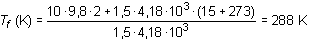
tf (C) = 288 - 273 = 15 C



