| Natureduca - Portal educativo de ciencia y cultura |

Química
LOS COMPUESTOS DEL CARBONO
Introducción - 1ª parte
El carbono en el Universo
 l
carbono es un elemento químico no metálico, integrado en
el grupo 14 de la tabla periódica. Aunque está
ampliamente distribuido en la naturaleza, el carbono no
es particularmente abundante (sólo representa el 0,025
por ciento de la corteza terrestre), sin embargo, forma
más compuestos que todos los demás elementos combinados.
Sobre la base del peso, el carbono es el decimonoveno en
orden de abundancia elemental en la corteza de la
Tierra, y se estima que en el Universo existen 3,5 veces
más átomos de carbono que átomos de silicio. Sólo el
hidrógeno, el helio, el oxígeno, el neón y el nitrógeno
son atómicamente más abundantes en el cosmos que el
carbono.
l
carbono es un elemento químico no metálico, integrado en
el grupo 14 de la tabla periódica. Aunque está
ampliamente distribuido en la naturaleza, el carbono no
es particularmente abundante (sólo representa el 0,025
por ciento de la corteza terrestre), sin embargo, forma
más compuestos que todos los demás elementos combinados.
Sobre la base del peso, el carbono es el decimonoveno en
orden de abundancia elemental en la corteza de la
Tierra, y se estima que en el Universo existen 3,5 veces
más átomos de carbono que átomos de silicio. Sólo el
hidrógeno, el helio, el oxígeno, el neón y el nitrógeno
son atómicamente más abundantes en el cosmos que el
carbono.
El carbono es el producto cósmico de la combustión de helio, en la que tres núcleos de helio, el número atómico 4, se fusionan para producir un núcleo de carbono, el número atómico 12.
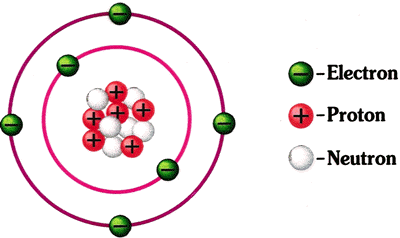
Electrónicamente el átomo de carbono tiene seis protones
y seis electrones (cuatro electrones en su capa de
valencia)
- Para más información sobre la configuración electrónica del carbono, véase el apartado: El átomo de carbono - 2ª parte
El carbono como referencia
En 1961, las organizaciones internacionales de física y química pura aplicada (IUPAP y IUPAC), seleccionaron el isótopo carbono-12 para reemplazar al oxígeno como el estándar con respecto al cual se miden los pesos atómicos de todos los demás elementos.
Por su parte, el carbono-14, que es radiactivo, es el isótopo utilizado en datación por radiocarbono y radiomarcaje. Se ha determinado que el carbono-14 tiene un periodo de desintegración de 5730 años, y dado que está presente en todas las materias orgánicas, es útil para realizar dataciones de esas materias.
Los compuestos del carbono
Aunque en la corteza de la Tierra el carbono elemental es un componente menor, sin embargo, los compuestos de carbono (es decir, carbonatos de magnesio y calcio) forman minerales comunes (como magnesita, dolomita, mármol o piedra caliza). El coral y las conchas de ostras y almejas son principalmente carbonato de calcio. El carbono se distribuye ampliamente en forma de carbón, y también en los compuestos orgánicos que constituyen el petróleo, el gas natural y todo el tejido vegetal y animal.

El carbón es una de las formas en que se distribuye el
carbono en la corteza terrestre. El carbón posee además
cantidades de otros elementos, como azufre, hidrógeno,
nitrógeno y oxígeno
Existe una secuencia natural de reacciones químicas llamada "ciclo del carbono", que constituye uno de los más importantes procesos biológicos; implica la conversión del dióxido de carbono atmosférico en hidratos de carbono por la fotosíntesis de las plantas, el posterior consumo de estos carbohidratos por los animales, y finalmente su oxidación a través del metabolismo, para producir dióxido de carbono y otros productos, retornando el éste a la atmósfera.
- Véase el apartado: El Ciclo del carbono
El descubrimiento del carbono
La palabra carbono proviene del latín "carbo" (carbón o brasa). El carbono como elemento fue descubierto probablemente por la persona que utilizó el fuego por primera vez; se tiene constancia del uso de carbón vegetal en pinturas rupestres con más de 15.000 años de antigüedad. Así, junto con el azufre, hierro, estaño, plomo, cobre, mercurio, plata y oro, el carbono era uno de los pequeños grupos de elementos bien conocidos en el mundo antiguo.

Briquetas de carbón vegetal
El carbón vegetal posee un alto contenido en carbono, alrededor de un 98%. Se produce cuando se somete materias vegetales, como la madera, a altas temperaturas con ausencia de oxígeno.
La química del carbono moderna data del desarrollo del carbón, petróleo y gas natural como combustibles, y de la elucidación de la química orgánica sintética, ambos fueron sustancialmente desarrollados desde el siglo XIX.



