| Natureduca - Portal educativo de ciencia y cultura |

Química
ENERGÍA Y REACCIÓN QUÍMICA
La espontaneidad de las reacciones químicas - 1ª parte
El principio de mínima energía
 omo en toda la naturaleza, también en las reacciones
químicas opera el principio de mínima energía según el cual los sistemas
materiales tienden a evolucionar en el sentido en el que disminuye su energía
potencial.
omo en toda la naturaleza, también en las reacciones
químicas opera el principio de mínima energía según el cual los sistemas
materiales tienden a evolucionar en el sentido en el que disminuye su energía
potencial.
Una bola rueda por un plano inclinado hasta encontrar la posición más baja, que es la de menor energía; un muelle comprimido se expande para conseguir una condición de mínima deformación y, por tanto, de mínima energía acumulada, y una reacción química evoluciona hacia estados de menor contenido energético.
Sucede, en ocasiones, que siendo el contenido energético de los productos inferior al de los reactivos, el sistema en cuestión no evoluciona espontáneamente como cabría esperar según el principio de mínima energía.
En una parte de los casos, esto es debido a que se precisa una cierta cantidad de energía, por lo general pequeña, para poner en marcha la reacción, de la misma manera que es preciso dar un impulso inicial a un bloque de madera para que descienda por un plano inclinado.
Esta dosis de energía inicial se denomina energía de activación y se emplea en la ruptura de los primeros enlaces, que suministrará energía propia suficiente como para mantener la reacción por sí misma.
El principio de máximo desorden
De acuerdo con el principio de mínima energía, considerado aisladamente, ninguna reacción endotérmica podría ser espontánea, pues en este tipo de reacciones la energía del sistema aumenta.
Sin embargo, existen en la naturaleza reacciones y procesos que, siendo endotérmicos, se producen espontáneamente. Ello indica que, junto con la energía, otro factor debe condicionar el carácter espontáneo de una reacción química. Ese factor adicional es el grado de desorden, también denominado entropía (S).
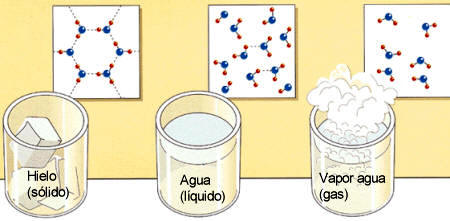
La entropía es una magnitud
que da idea del grado de desorden molecular de un sistema. El paso de hielo
a agua líquida y de ésta a vapor de agua aumenta el valor de la entropía del
sistema.
La entropía depende de factores tales como el número de partículas en juego o el estado físico de las sustancias. Así el estado gaseoso es más desordenado que el líquido o que el sólido y corresponde, por lo tanto, a una mayor entropía.
Junto con la tendencia a alcanzar el estado de mínima energía, los sistemas químicos tienden de forma natural a alcanzar el estado de máximo desorden y son ambos factores los que controlan conjuntamente el carácter espontáneo de las reacciones químicas.



