| Natureduca - Portal educativo de ciencia y cultura |

Química
EL LENGUAJE QUÍMICO
Introducción - 2ª parte
Conceptos fundamentales (continuación)
Número de oxidación
 e forma general y a efectos de formulación, a cada elemento dentro de un
compuesto se le asigna un número positivo o negativo denominado índice, número o
grado de oxidación. Dicho índice, que puede considerarse como el número de
electrones perdidos o ganados en el ion correspondiente (en el supuesto de que
todos los compuestos fueran iónicos) tiene, no obstante, un carácter
fundamentalmente operativo, pues sirve para deducir con facilidad las fórmulas
de las diferentes combinaciones posibles.
e forma general y a efectos de formulación, a cada elemento dentro de un
compuesto se le asigna un número positivo o negativo denominado índice, número o
grado de oxidación. Dicho índice, que puede considerarse como el número de
electrones perdidos o ganados en el ion correspondiente (en el supuesto de que
todos los compuestos fueran iónicos) tiene, no obstante, un carácter
fundamentalmente operativo, pues sirve para deducir con facilidad las fórmulas
de las diferentes combinaciones posibles.
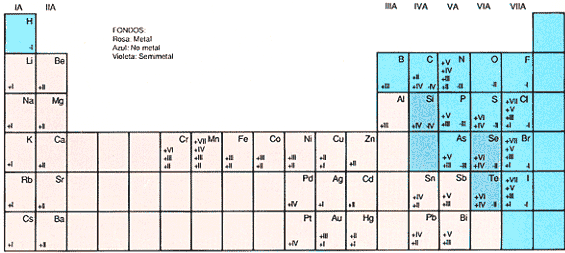
La tabla muestra los números de oxidación que se asignan a los elementos de más importancia. Cuando se analiza con detenimiento se advierte la existencia de ciertas relaciones entre el índice de oxidación de un elemento y su posición en el sistema periódico de modo que es posible deducir las siguientes reglas básicas:
a) Los elementos metálicos tienen índices de oxidación positivos.
b) Los elementos no metálicos pueden tener índices de oxidación tanto positivos como negativos.
c) El índice de oxidación positivo de un elemento alcanza como máximo el valor del grupo (columna) al que pertenece dentro del sistema periódico. En el caso de que tome otros valores, éstos serán más pequeños, soliendo ser pares o impares según el grupo en cuestión sea par o impar.
d) El índice de oxidación negativo de un elemento viene dado por la diferencia entre ocho y el número del grupo al que pertenece dentro del sistema periódico.
Es preciso aclarar que estos números se asignan a los diferentes elementos cuando se hallan formando un compuesto. El índice de oxidación de un elemento sin combinar es cero.
Al igual que sucedía con los símbolos, los números de oxidación deben memorizarse, puesto que junto con aquéllos constituyen los elementos básicos de toda la formulación química. Es conveniente hacerlo por grupos de elementos con igual índice de oxidación, ya que cuando elementos diferentes actúan con idénticos índices de oxidación, dan lugar a fórmulas totalmente análogas.



