| Natureduca - Portal educativo de ciencia y cultura |

Química
ACIDEZ Y BASICIDAD
Conceptos actuales de ácido y base - 2ª parte
Definición de Brônsted-Lowry
 a disociación de un ácido genérico de fórmula AH en un medio
acuoso, lleva consigo la cesión de un H+ a una molécula de agua según una
reacción del tipo:
a disociación de un ácido genérico de fórmula AH en un medio
acuoso, lleva consigo la cesión de un H+ a una molécula de agua según una
reacción del tipo:
AH + H2O < > H3O+(aq) + A-(aq)
Pero el H+ es un átomo de hidrógeno que ha perdido su electrón; es por tanto un protón, de modo que el ácido ha cedido un protón durante el proceso.Razonamientos de este estilo llevaron al químico danés J.N. Brönsted (1879-1947) a proponer la siguiente definición de ácido:
"Ácidoes toda sustancia capaz de ceder uno o más protones a otra molécula" Al proponer este nuevo concepto de ácido, Brönsted buscaba una definición que se pudiera relacionar con la correspondiente de base, tal y como lo estaban las propiedades químicas de ambos tipos de sustancias. Puesto que un ácido tiene propiedades opuestas a las de una base, la definición de base debería reflejar una propiedad opuesta a la del ácido. Así, de acuerdo con la definición de Brönsted:
"Basees una sustancia capaz de aceptar uno o más protones de otra molécula" El comportamiento del amoníaco (NH+) se explica como consecuencia de la siguiente reacción con el agua:
![]()
![]()
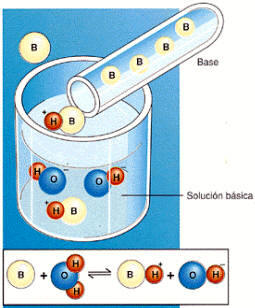
Según la definición de Brônsted, una base B es
toda sustancia aceptora de protones. En disolución acuosa, B acepta un
protón del agua y se convierte en BH+liberando grupos OH+al medio.



